Reeds op 24 Augustus 2021 het Cara Therapeutics en sy sakevennoot Vifor Pharma aangekondig dat sy eerste-in-klas kappa-opioïedreseptor-agonis difelikefalin (KORSUVA™) deur die FDA goedgekeur is vir die behandeling van pasiënte met chroniese niersiekte (CKD) (positiewe matige/ernstige pruritus met hemodialysebehandeling), en dit sal na verwagting in die eerste kwartaal van 2022 bekendgestel word. Cara en Vifor het 'n eksklusiewe lisensieooreenkoms onderteken vir die kommersialisering van KORSUVA™ in die Verenigde State en ooreengekom om KORSUVA™ aan Fresenius Medical te verkoop. Onder hulle het Cara en Vifor elk 'n winsaandeel van 60% en 40% in verkoopsinkomste anders as Fresenius Medical; elk het 'n winsaandeel van 50% in verkoopsinkomste van Fresenius Medical.
CKD-geassosieerde pruritus (CKD-aP) is 'n algemene pruritus wat met 'n hoë frekwensie en intensiteit voorkom by CKD-pasiënte wat dialise ondergaan. Pruritus kom voor in ongeveer 60%-70% van pasiënte wat dialise ontvang, waarvan 30%-40% matige/ernstige pruritus het, wat die lewensgehalte ernstig beïnvloed (bv. swak slaapgehalte) en met depressie geassosieer word. Daar is nog geen effektiewe behandeling vir CKD-verwante pruritus nie, en die goedkeuring van Difelikefalin help om die groot mediese behoeftegaping aan te spreek. Hierdie goedkeuring is gebaseer op twee deurslaggewende Fase III kliniese proewe in die NDA-indiening: positiewe data van die KALM-1 en KALM-2 proewe in die VSA en wêreldwyd, en ondersteunende data van 32 bykomende kliniese studies, wat toon dat KORSUVA ™ goed verdra word.
Nie lank gelede nie, het goeie nuus gekom uit die kliniese studie van difelikefalin in Japan: 2022-1-10 het Cara aangekondig dat sy vennote Maruishi Pharma en Kissey Pharma bevestig het dat difelikefalin-inspuiting in Japan gebruik word vir die behandeling van pruritus by hemodialyse-pasiënte. Fase III kliniese proewe Die primêre eindpunt is bereik. 178 pasiënte het 6 weke difelikefalin of placebo ontvang en deelgeneem aan 'n 52-week oop-etiket verlengingsstudie. Die primêre eindpunt (verandering in pruritus numeriese graderingskaaltelling) en sekondêre eindpunt (verandering in jeuktelling op die Shiratori Ernstigheidskaal) was beduidend verbeter vanaf die basislyn in die difelikefalin-groep in vergelyking met die placebo-groep en is goed verdra.
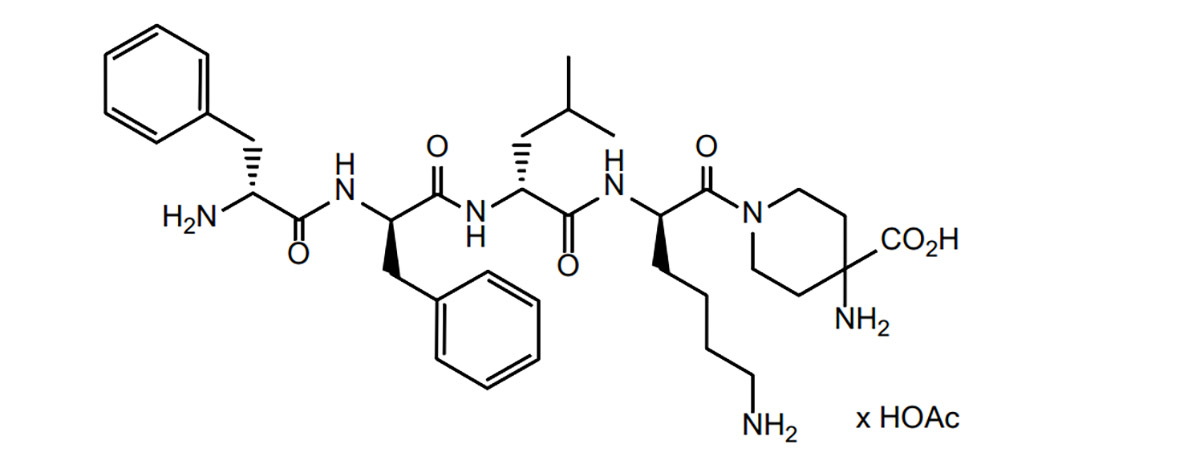
Difelikefalin is 'n klas opioïedpeptiede. Gebaseer hierop het die Peptide-navorsingsinstituut die literatuur oor opioïedpeptiede bestudeer en die probleme en strategieë van opioïedpeptiede in geneesmiddelontwikkeling opgesom, sowel as die huidige geneesmiddelontwikkelingsituasie.
Plasingstyd: 17 Februarie 2022